Principe actif : le Pimobendane
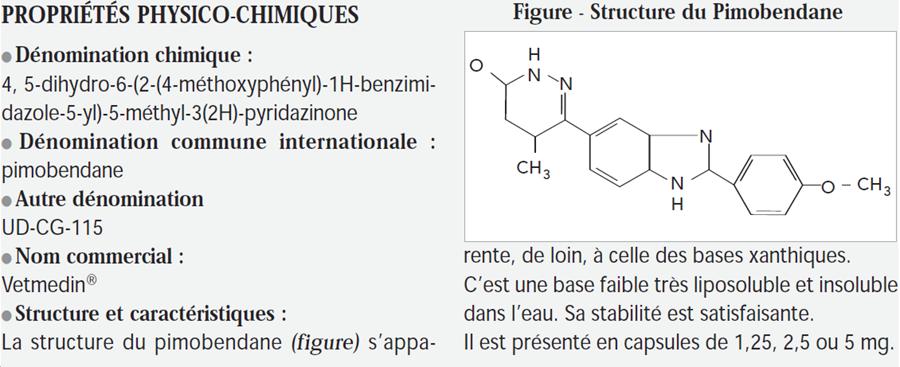
Molécule dérivée de la famille chimique des benzimidazoles, le pimobendane fait partie de la classe thérapeutique des inodilatateurs.
Ses propriétés principales sont un effet inotrope positif cardiaque et un effet vasodilatateur artérioveineux [26].
Cette classe comprend deux grandes familles, les inhibiteurs de la phosphodiestérase III (I.P.D.E. III) et les sensibilisateurs calciques.
Les inhibiteurs de la phosphodiestérase III permettent l’inhibition de la dégradation de l’AMPc par inhibition intracellulaire spécifique de cette enzyme.
- Au niveau cardiaque, la conséquence est une ouverture des canaux calciques membranaires et la libération de calcium par le réticulum sarcoplasmique. Le taux intracellulaire de calcium s’élève, ce qui facilite la contraction cardiaque (action sur la cellule cardiaque). Néanmoins, cette augmentation de la concentration intracellulaire calcique est délétère pour la cellule cardiaque, car elle s’accompagne d’une élévation de la consommation en oxygène par la cellule [21].
- Au niveau vasculaire, l’augmentation du taux d’AMPc inhibe la “myosin light-chain kinase“ et favorise la recapture du calcium intracellulaire par le réticulum sarcoplasmique, inhibant ainsi l’interaction actinemyosine, ce qui entraîne une vasodilatation artérielle et veineuse (action sur la cellule musculaire lisse vasculaire).
Les sensibilisateurs calciques agissent différemment. Ils facilitent l’interaction entre la troponine C et le calcium dans les cardiomyocytes, donc ils entraînent une meilleure utilisation du calcium intracellulaire présent pour le couplage actine-myosine [8, 22]. Cette utilisation facilitée favorise la contraction cardiaque (action sur la cellule cardiaque), sans augmenter la concentration intracellulaire de calcium. Ils ont aussi une action vasodilatatrice, qui s’exerce par différents mécanismes (inhibition des phosphodiestérases, inhibition des canaux calciques, activation des canaux potassiques).
Pharmacologie
Pharmacocinétique
- Chez le chien, la résorption orale du pimobendane est rapide et incomplète. Le pic plasmatique est atteint en une heure après administration orale, mais sa biodisponibilité est de l’ordre de 60 p. cent. Celle-ci est encore diminuée s’il est administré pendant ou peu de temps après le repas : aussi, faut-il l’employer au moins une heure avant.
- Sa distribution est large, avec un volume de distribution de 2,6 l/kg. Le pimobendane est fortement fixé aux protéines plasmatiques. Les transformations hépatiques du composé conduisent à la formation d’un métabolite actif, surtout inhibiteur des phosphodiestérases.
- La demi-vie du pimobendane est d’environ 25 min, celle de son métabolite actif est de 2 h. Mais en raison de sa large distribution et de son affinité pour le myocarde, ses effets se prolongent pendant 8 h environ.
- L’élimination est principalement biliaire. La dose d’emploi ne doit donc pas être modifiée en cas d’insuffisance rénale.
Pharmacodynamie
Effet inotrope positif
Le pimobendane est un sensibilisateur calcique qui exerce son effet inotrope sans augmentation de la concentration intracellulaire de calcium, donc sans augmenter la consommation en oxygène du myocarde [21]. De plus, cette molécule améliore la fonction systolique par un renforcement de la contractilité cardiaque, sans entraîner les effets secondaires qui peuvent être rencontrés avec les autres molécules inotropes (milrinone, amrinone, …), qui augmentent la concentration intracellulaire calcique, et accroissent le risque de survenue de troubles du rythme cardiaque [27].
Cet effet inotrope positif est stable dans le temps, alors que les inotropes purs (inhibiteurs de la phosphodiestérase III) perdent de leur efficacité avec l’évolution de l’insuffisance cardiaque, en raison de la baisse d’expression des récepteurs béta-adrénergiques au niveau cardiaque [2, 22, 23].
Effet vasodilatateur
L’effet vasodilatateur du pimobendane est double. Il existe un effet vasodilatateur systémique artériel et veineux, et un effet vasodilatateur coronarien.
Un effet vasodilatateur systémique : l’effet vasodilatateur du pimobendane est surtout lié à son effet inhibiteur des phosphodiestérases, qui réduit l’activité des myofilaments contractiles (inhibition de la myosine light chain kinase), mais qui diminue aussi la concentration de calcium intracellulaire en :
- stimulant sa recapture par le réticulum sarcoplasmique;
- inhibant les canaux calciques de type L ;
- activant les canaux potassiques [4, 8, 26, 27].
Un effet vasodilatateur coronarien : le pimobendane augmente les flux coronariens subépicardiques, intramyocardiques et transmuraux [8, 19].
Effet lusitrope positif
- Le lusitropisme représente la capacité de relaxation du myocarde en phase de diastole ventriculaire. Un lusitropisme positif signifie l’amélioration de la relaxation, favorisant ainsi le remplissage diastolique.
- Le pimobendane possède cet effet lusitrope positif [1]. Néanmoins, les mécanismes précis de cette propriété ne sont pas encore complètement élucidés.
Effets neuro-hormonaux
- Le pimobendane permet la diminution de la concentration du TNF-alpha et des interleukines 1b et 6 [9].
- Cet effet est potentiellement bénéfique, car la présence de ces cytokines pro-inflammatoires s’accompagne d’une augmentation de la morbidité et de la mortalité.
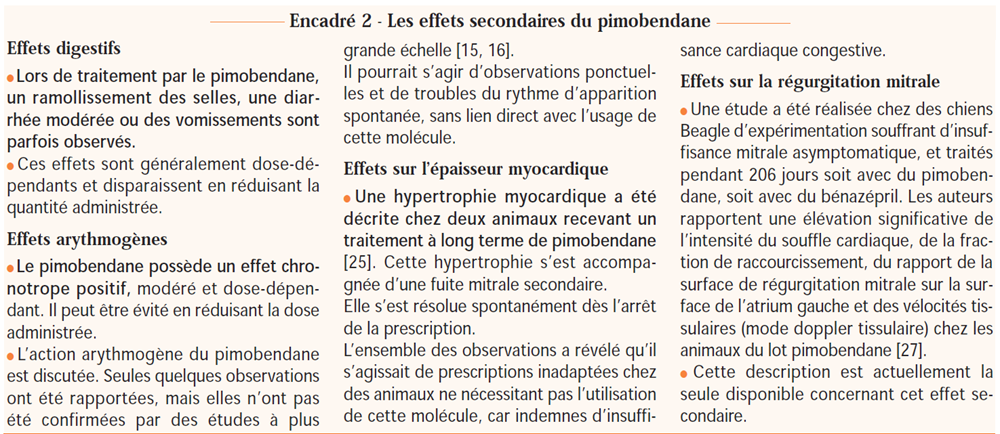
Effets secondaires
- Comme tout médicament, le pimobendane est susceptible d’avoir des effets secondaires indésirables.
- Les quatre principaux sont des effets digestifs, arythmogènes, hypertrophiants sur le myocarde, sur la fuite mitrale lors de maladie valvulaire chronique (encadré 2).

Usage thérapeutique
Le traitement des cardiomyopathies dilatées et des affections valvulaires chroniques
L’ensemble des propriétés décrites permet d’envisager une utilisation clinique raisonnée du pimobendane dans les cardiopathies du chien.
Les principales cardiopathies concernées par ce traitement sont les cardiomyopathies dilatées et les affections valvulaires chroniques. L’évolution systématique de ces deux types de maladies cardiaques est l’insuffisance cardiaque (encadré 1).
Les effets pharmacologiques décrits font du pimobendane une molécule préconisée pour le traitement de l’insuffisance cardiaque :
- son effet vasodilatateur artériel permet la réduction de la post-charge systémique et des pressions artérielles pulmonaires et son effet vasodilatateur veineux diminue la précharge (baisse de la pression veineuse hydrostatique) [26] ;
- son effet vasodilatateur coronarien entraîne une meilleure oxygénation myocardique ;
- son effet inotrope positif permet une correction de la chute de contractilité, présente précocement lors de cardiomyopathie dilatée. Lors de maladie valvulaire chronique, la baisse de contractilité, n’est détectable que tardivement dans l’évolution de la maladie, par les méthodes classiques d’imagerie (échocardiographie conventionnelle) ;
- son effet lusitrope permet l’amélioration du remplissage diastolique.
Le pimobendane est actuellement, enregistré dans toute l’Europe. L’indication mentionnée par l’A.M.M. est le “traitement de l’insuffisance cardiaque congestive due à une cardiomyopathie dilatée ou à une insuffisance valvulaire (mitrale et tricuspide), si nécessaire en association avec un diurétique (furosémide)“. La dose établie est de 0,25 mg/kg per os toutes les 12 heures.
Les données sur les cardiomyopathies dilatées
Lors de cardiomyopathie dilatée, les principales études réalisées révèlent que le pimobendane augmente la qualité et la durée de vie [5, 10, 11, 17].
En particulier, chez des Dobermans atteints de cardiomyopathie dilatée en phase clinique, l’espérance de vie est de 64 +/- 14 jours en moyenne avec un traitement composé de furosémide, d’un inhibiteur de l’enzyme de conversion de l’angiotensine (I.E.C.A.) et d’un placebo, alors qu’elle est de 128 +/-29 jours en moyenne avec un traitement à base de furosémide, d’inhibiteur de l’enzyme de conversion de l’angiotensine et de pimobendane [17].
Ces résultats sont confirmés par l’étude de Fuentes, qui établit une médiane de survie de 329 jours (avec un intervalle de 42 à 393 jours) lors de l’administration de pimobendane chez des Dobermans atteints de cardiomyopathie dilatée associée à une insuffisance cardiaque, et déjà traités avec du furosémide, un inhibiteur de l’enzyme de conversion de l’angiotensine et de la digoxine, contre 50 j (avec un intervalle de 13 à 196 j) pour ceux qui reçoivent un placebo [5].
La seule exception à l’augmentation de la durée de vie par l’utilisation du pimobendane est la forme développée par le Cocker spaniel, dont l’évolution n’est pas ralentie [5]. La qualité de vie est cependant améliorée dans cette race.
L’utilisation du pimobendane dans la cardiomyopathie dilatée doit s’envisager à partir du stade 2 de l’insuffisance cardiaque, car aucune étude n’a démontré son intérêt dans les stades asymptomatiques, contrairement aux inhibiteurs de l’enzyme de conversion de l’angiotensine [14].
Les données sur les affections valvulaires chroniques
Lors de maladie valvulaire mitrale, des études montrent que l’utilisation du pimobendane est aussi efficace que celle d’un inhibiteur de l’enzyme de conversion de l’angiotensine, pour la qualité de vie et sa durée [13, 18, 20, 24].
En particulier, la proportion d’événements indésirables (incluant la mort ou l’euthanasie) est inférieure chez des chiens insuffisants cardiaques traités avec du furosémide et du pimobendane par rapport à ceux traités avec du furosémide et du ramipril [24].
De même, selon une communication de Ripken, le confort de vie est amélioré très rapidement avec le pimobendane, avec une espérance de vie identique à celle observée avec un inhibiteur de l’enzyme de conversion de l’angiotensine, pour des doses de furosémide associées inférieures [20].
Une étude très récemment publiée établit, chez 76 chiens insuffisants cardiaques, une nette amélioration des scores d’insuffisance cardiaque à 56 j, selon la classification de l’International Small Animal Cardiac Health Council (I.S.A.C.H.C.), dans le groupe traité au pimobendane et au furosémide, par rapport au groupe traité au bénazépril et au furosémide [13]. Concernant l’espérance de vie au-delà de 56 j, la médiane est de 415 j dans le groupe pimobendane, contre 128 jrs dans le groupe bénazépril.
Une étude actuellement en cours, dont les résultats devraient être connus courant 2007, va probablement permettre de mieux préciser les cadres d’utilisation de cette molécule [3] : celle-ci comprend 260 chiens atteints d’endocardiose valvulaire associée à une insuffisance cardiaque (stade 2 de la classification I.S.A.C.H.C.) et traités soit avec du pimobendane, soit avec du bénazépril.
Le pimobendane apparaît ainsi efficace, bien toléré, et présente un intérêt complémentaire dans le traitement de l’insuffisance cardiaque congestive secondaire à une maladie valvulaire mitrale. Certains auteurs avancent un possible intérêt de cette molécule en phase aiguë, compte tenu de sa rapidité d’action (le pic d’effets hémodynamiques intervient une heure après une administration orale à jeun) [22].
En revanche, comme pour les inhibiteurs de l’enzyme de conversion de l’angiotensine, aucune étude publiée à ce jour ne justifie l’utilisation du pimobendane sur les stades asymptomatiques d’insuffisance cardiaque.
L’utilité d’une polythérapie
- Qu’il s’agisse d’une maladie valvulaire chronique ou d’une cardiomyopathie dilatée, le traitement de l’insuffisance cardiaque congestive peut nécessiter une polythérapie (inhibiteurs de l’enzyme de conversion de l’angiotensine, diurétiques, antiarythmiques, …). Il est possible, dans de bonnes conditions de sécurité, en particulier afin de préserver la fonction rénale, d’inclure le pimobendane dans l’arsenal thérapeutique [12]. Les nombreuses études de comparaison avec les inhibiteurs de l’enzyme de conversion de l’angiotensine en apportent la justification, car elles impliquent des polythérapies.
- En revanche, les effets de l’association, potentiellement intéressante, entre pimobendane et inhibiteurs de l’enzyme de conversion de l’angiotensine ne sont pas connus. Sur un plan physiopathologique, l’association de ces deux vasodilatateurs de modes d’actions différents apparaît bénéfique. Néanmoins, aucune étude n’est disponible à l’heure actuelle pour évaluer cette synergie.
Conclusion
- Par son mécanisme d’action original et complexe, associant des effets inotropes, lusitropes, vasodilatateurs artérioveineux et coronariens, le pimobendane présente un intérêt pour traiter l’insuffisance cardiaque congestive, secondaire à une cardiomyopathie dilatée ou à une maladie valvulaire mitrale.
- La littérature scientifique disponible démontre son efficacité et sa sécurité d’emploi, qu’il soit utilisé seul ou en association avec des diurétiques ou d’autres médicaments classiques de l’insuffisance cardiaque (inhibiteurs de l’enzyme de conversion de l’angiotensine, digoxine, anti-arythmiques). Les études en cours devraient permettre de mieux préciser encore
le cadre de son utilisation.